![]()
���Ղ̕���(���ՂƎv���錻�ۂ̒��ɂ��Ȃ�̕p�x�Ō���܂��)
���Ղ̌����̈�ɕ��H������܂����ʓI�ɖ��ՂƂ����Ɩ��C�ɂ�餕����̌��������Ӗ�����悤�ɍl����ꂪ���ł�����Ⴆ�Τ�d�������ŏ_�炩���Ώە�������Ă���ɂ�������炸����Ղ��������Ȃ錻�ۂ����邱�Ƃ������Ǝv���܂�����̗l�ȏ�Ԃ̃��[�N�������グ�Ē������Ă݂�ƁA���C�ɂ�閁�Ղ����ނ��땅�H�ɂ��Ǝ㉻�A���邢�͒E���ɂ�閁�Ղ�������܂����Ȃ̂ͤ�����̌����ł����閁�Ղɂ͂��܂�A��肴������邱�Ƃ��Ȃ������s���̂܂܈Ⴄ�ގ��Ɉڍs���ꂽ�褍d�x���グ������Ŏ��H��̐v���̂�ύX���Ă��܂����Ƃ��������Ƃł�������́A�g�p���������̓����⑊���A���邢�͌��ۂ̗v�������炩���ߗ�������Ă���A�w�ǂ��h������̂ł�����Ӗ��Ȏ��ԂƔ�p�̘Q�������邽�߂Ɉ�x�A�����ޗ��̕��H�ɂ��ĐG��Ă݂����Ǝv���܂��
�����̕��H���ۂ��̂��̂͋��������猩��Τ���̃C�I�������邢�͎_�������ŁA����ʂł͂���߂ĒP���Ȕ����ł�����������p�����ޗ����x���ł̍ޗ����̊e��̕s�ψꐫ����сA���ꂪ������Ă�������̏����̑��l���̂䂦�Ɍ��ʂƂ��Č���镅�H�̌��ۂ͂���߂ĕ��G�ƂȂ褕��H�`�Ԃ����ɗl�X�ƂȂ�܂�����H�`�Ԃ͋ψꕅ�H�ƕs�ψꕅ�H�����������Τ�S�ʕ��H�ƋǕ����H�ɑ�ʂł��܂���܂����H���ۂɉe��������q�ɂ͍ޗ������q�Ɗ������q�̑o��������̂ŁA���H�`�Ԃ��ψ�ɂȂ邩��s�ψ�ɂȂ邩�͍ޗ����A�����܂��͂��̑o�����ψꉻ��s�ψꂩ�Ɉˑ�����Ƃ����܂���s�ψꐫ�̗�Ƃ��čޗ����ł͊i�q���ׁA���ׂ�ʤ�������E�A�W���g�D�A�ΐ͕�����H����c�����ͤ�Ȃǂ�����A�����ł͋z���w��g�U�w��f�|�W�b�g����H�������������������x����}�N���Z���Ȃǂ��������܂��
�S�ʕ��H
�ψꕅ�H�܂��͑S�ʕ��H�͕��H�̍ł���{�I�Ȍ`�Ԃł��邪��K�������ǂ̖ʂ��S������̑��x�ŗn������킯�ł͂Ȃ��"��r�I�ψ�ȕ��H��"���c���Ƃ������x�̂��̂��܂܂�顎��n�����ł͎g�p���������ޗ��̑����͕s���ԋ����ł���̂Ť����炪�s���ԉ��ł��������Ԃŕ��H����Ƃ��ɒ悷�镅�H��Ԃ���\�I�ȑS�ʕ��H�ōł����Ⴊ�����
���H���S�ʤ�ψ�ɐi�ނ��߂ɂͤ�����̑ϐH���ɔ�ׂĊ��̕��H�����啝�ɏ��褕��H���x���傫���Ȃ邱�Ƃ������ɂȂ顂���ɂ�蕅�H�������������\�ʂɂƂǂ܂ꂸ�n�t���ɗn������̂ł��̌�̔����ɖ��W�ɂȂ褂܂��������̏��X�̕s�ψ�v�������H�̑S�v���Z�X�ɂقƂ�lje�����Ȃ��Ȃ�̂ŕ��H�͋ψꤑS�ʂɐi�s���顊_���̓S�ȂǤ���_���̋����̊����ԕ��H����\�I�ł���
�������S�ʕ��H�Ƃ͂������H�ʂ��S���ψ�ɋ��̖ʂ̂悤�ɐi�ނ��Ƃ͂܂�Ť�f�n�����̌����\����g�D�̉e�����ăU���U���ȖʂɂȂ����藜�n�l�̕\�ʂ��c�����Ƃ���������ʂ̂悤��"�ψ�"���H�͓d�������̂悤�ɗn�o�C�I���̊g�U�������ɂȂ�قǂ̑呬�x�ŗn��������f�n�����̍\����g�D�
�`��Ȃǂ��S���e�����Ȃ��Ȃ�Ƃ��ɂ̂����
�S�ʕ��H�ͤ���H���x�����Ԃɑ��قڈ��Ő��ڂ���̂ł��̗\���͊����ȒP�Ť�Z���Ԃ̐N�Е��H������d�C���w�I���ɑ���ŕ��H���x��ϐH������]���ł���
�S�ʕ��H�ɑ���h�H��ɂ��Ăͤ�������������̑ϐH�����S���s�����Ă���̂������ł���̂ōޗ��I����l���������Ƃ���{�ł��顉��}�I�ɂ̓C���q�r�^�[�̓Y����d�C�h�H�̓K�p�Ȃǂ��l������
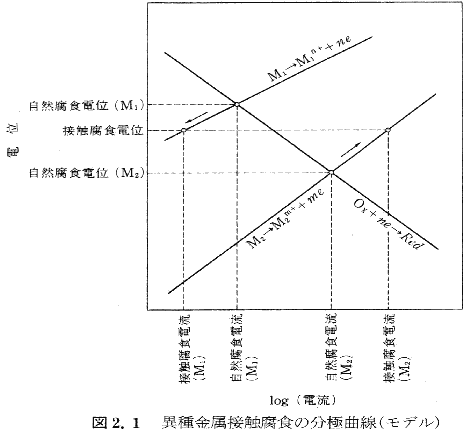
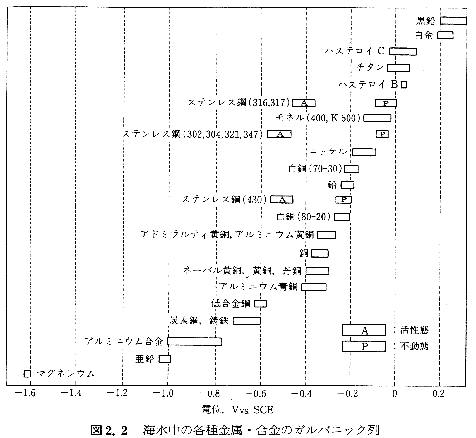
| �َ�����ڐG���H ���R���H�d�ʂɍ��̂�����̋�����ڐG���Ďg�p����ƕ��H�d�ʂ��ڂȋ����̕��H�����i���ꤋM�ȋ������t�ɖh�H����錻�ۂ�������K���p�j�b�N���H�Ƃ��Ă�顂����Ŗ��ƂȂ�d�ʂ͂����܂ł����H�d�ʁi�����d�ʁj�ł�������̃C�I�����̉t�d�ʁi���t�d�ʁj�ł͂Ȃ����Ƃɒ��ӂ��顃X�e�����X�|�̉������Ǖ����H�ɂ����銈���ԁ^�s���ԓd�r���H�Ȃǂ����̋@�\�̈��ƍl����ꤕK�����������̎�ނ��قȂ�Ȃ��Ă����̕��H���i�@�\�͐��藧�¡�َ�����ڐG���H�ɂ��ڂȋ����̕��H�����i���������f�����ɋȐ��ɂ���Đ}2.1�Ɏ���� ���̂Ƃ��̐ڐG���H�d�ʂ͑o���̋����̎��R���H�d�ʂ̊Ԃ̂ǂ����ɗ�����������̓d�ʂ͊W���邷�ׂĂ̓d�C���w�n�̃A�m�[�h�������x�̑��a�ƃJ�\�[�h�������x�̑��a���������Ȃ�d�ʂƂ��Č��߂��顂��Ȃ킿�����̕��H�n�̕��������d�ʂƂ������� ��X�̋����ɂ��Ĥ���̃C�I�����̉t�d�ʂ������悭���ׂ��V���[�Y��W���d�C���w��i���w�ł����C�I�����X���j�Ƃ����̂ɑ�����̊����ł̕��H�d�ʂ̂�����K���o�j�b�N��Ə̂��顊C�����ł̎�X�̋���������̃K���o�j�b�N��̗��}2.2�j�Ɏ���� ���̓d�ʍ��͂������َ�����ڐG���H�ɑ傫�ȉe�����y�ڂ����q�ł��邪����ꂾ���ŕ��H�̒��x�����܂�킯�ł͂Ȃ���ł��傫�ȗv���͒P�Ƃ̎��R�d�ʂ���ڐG���H�d�ʂ܂ŕ��ɂ����Ƃ��ɂǂ̂悤�ȕ��ɓ������������Ť��������߂镪�ɉߓd����n�t�̓d���x��ʐϔ䤋����Ȃǂ𑍍��I�ɍl������K�v������ �َ�����ڐG���H�łͤ�ڂȋ����̕��H�����i����M�ȋ������h�H�����̂���ʓI�ł��邪��s���ԋ����ł͕K�����������Ȃ�Ȃ����Ƃ����顃`�^���ƃ`�^���[�p���W�E��������ڐG�������Ƃ���M�ȓd�ʂ������o���W�E�������̕��̓d�ʂ��������ĕs����s���Ԉ�ɓ��褏��`�^���ƕς��Ȃ����������H���������Ⴊ����Ă��� �َ�����ڐG���H�̖h�~ �����ʂ�َ������ڐG�����Ďg�p���Ȃ����Ƃ���{�Ť��ނ����Ȃ��Ƃ��͗��҂�d�C�I�ɐ≏���顂����������ɂ͍ޗ��̋@��I��������H���Ȃǂ̐���َ���������p����������Ȃ���͑�������̂悤�ȏꍇ����ɓ������݂Ď��Q�̂Ȃ��g�ݍ��킹��I�Ԃ��Ƃ͂�����x�\�Ť��T�ɂ����r�����邱�Ƃ����ɐ_�o���W������K�v�͂Ȃ���t�Ɉَ�����ڐG���H��ϋɓI�ɗ��p�����Ƃ��Ĥ�]���z�ɂɂ��J�\�[�h�h�H�����顐}2.1�ɂ�����Ml��S�CM2���A���~�j�E���������}�O�l�V�E���Ȃǂ̍����̋]���z�ɂƂ���Ƥ�����̋]���I�n���ɂ���ēS���h�H�������悭�����ł��� |
|
 |
 |
�E�H
���R�\�ʏ�ő啔���̕\�ʂ����S�ȕs���Ԃ�ۂ��Ă���ɂ�������炸���������ꂽ�����ɂ����s�b�g��ɕ��H���i�s����`�Ԃ�������s���Ԍ^�̑����̋���������Ɍ���ꤑ����̏ꍇ���f�C�I���Ȃǂ̐N�H���A�j�I���̑��݉��Ő������額E�H�̑S�ߒ��͔疌�j��ߒ��i�����ߒ��j�Ƃ��̌�̐����ߒ��ɖ��m�ɕ������顂����ł̓X�e�����X�|�̉��������ł̍E�H�ɒ��ڂ�����̗��ߒ������Ă������Ƃɂ���
�i1�j�E�H�̔����Ɛ���
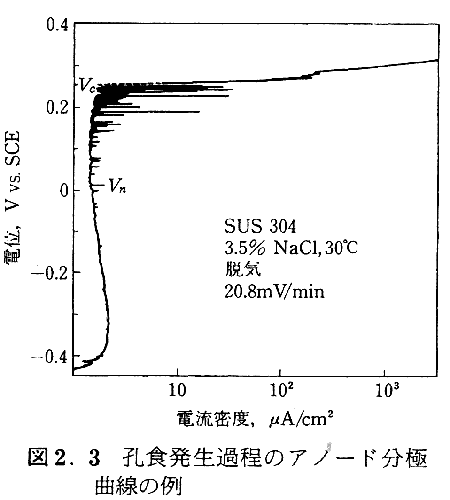
���R�\�ʂ���E�H����������ɂ͍|�����̗ՊE�E�H�d�ʁiVc�j���M�ɏ㏸�����邱�Ƥ���Ȃ킿����������x�_�����ł��邱�Ƃ��K�v�ł��額E�H�����ߒ��̃A�m�[�h���ɋȐ��̗��}2.3�Ɏ�����E�H�d�ʂ����ڂȓd�ʈ�ɔ疌�j��ƏC���ɔ����d���̐U��������ꤍE�H�d�ʂ��疌���̂��̂Ɖ��f�C�I���̑��ݍ�p�����łȂ��v�����܂ނ��Ƃ��������額E�H�d
�ʂ͂����܂Ȃǂ̊w�I�ȏ�ǂ̏�������邱�ƂȂ�����R�\�ʂ��玩�G�}��p�n�����N�������߂̏�ǂ���肾�����߂ɕK�v�ȍŒ�̓d�ʂł���Ɨ�������顂��̂悤�ɍE�H�d�ʂ͔疌�j��ߒ��ɑ������������ߒ��Ɋւ������l�Ȃ̂Ť�\�ʏ�Ԃ̑����̈Ⴂ�ɂ���ĉe�����ω����顂��̂��ߑ����̍E�H�d�ʂ̑���f�[�^�͓��v�I�ɂ���{����L���Ă��邪����̒l�͍E�H�̔����̗\����ύE�H���̕]���Ȃǂɂ����Ď��p��\���ɖ𗧂�����Ă����
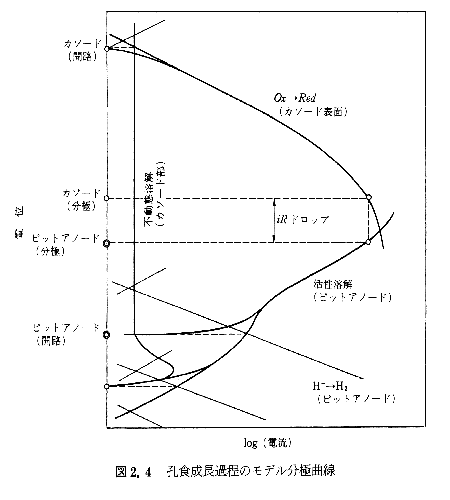
�����ߒ��ɂ���E�H�n�̃��f�����ɋȐ���}2.4�Ɏ������pH�C��Cl-�Z�x�ɕω������s�b�g�����̃A�m�[�h���ɋȐ��Ƥ���ӂ̐���ȕ\�ʂɂ�����_���܊Ҍ��̃J�\�[�h���ɋȐ����琬�褈��̃K���o�j�b�N���H�d�r���`�����čE�H����������
 |
 |
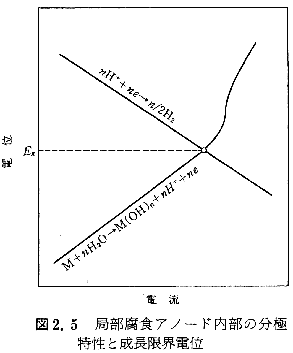
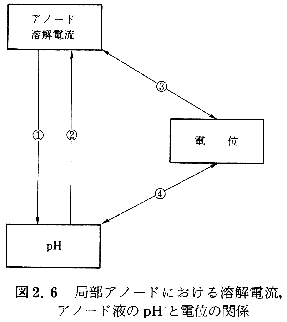
| �i2�j�������E�d�� �E�H�������ɐ����������邩�ۂ��͋Ǖ��A�m�[�h�ł̕��H�������̐������x �ƎU�푬�x�̑��ΓI�W�Ō��܂褌�҂��O�҂�菟��ƍE�H�͕s����������~���顕��H�������͋����̃A�m�[�h�n���ɂ�苟�����������C�I������{�Ť���̉��������ɂ�萶������H�{�Ƥ�����J�`�I���̒~�ςɌ������������O�����j�����Ă��Ē~�ς���Cl-�ő�\���꤂��̐������x�͍E�H�̃A�m�[�h�n�x���̂��̂Ō��܂顁i2.1�j�����U�푬�x�͋Ɍ��I�Ȋw�`����l���g�U���Ȃ��Ƃ���Ə㎮�Ő����������f�C�I���̃J�\�[�h�Ҍ��������x�Ō��܂顁i2.2�j�����͕s�t�I�Ȑ��f�d�ɔ������\��������̍����d�ʂ��������E�d�ʂɑ������顂���ɋȐ��̌`�Ő}2.5�Ɏ���� �Ǖ��A�m�[�h�ɂ�����n��d������уA�m�[�h�t�̕��H�����\����pH�Ɠd�ʂƂ̊W�� �}2.6�Ɏ���������Ť�@�A�m�[�h�n��d���������Ƌ����C�I���Z�x����������̉��������ɂ��H�{��������pH���ቺ���顇ApH�̒ቺ�͋Ǖ��A�m�[�h�\�ʂɐ������ׂ��疌�̗n��x���グ��n��d���傳���顇@�ƇA�̏z�T�C�N�������G�}��p�̖{���Ť��������Cl-�͋����C�I���̍����܂ƂȂ��Ĕ疌�`����h����܂�H�{�̊��ʂ��グ�Ĥ���̎��G�}�T�C�N���𑤖ʂ�菕�����顇B�ƇC���i2.1�j������сi2.2�j���̕��ɓ����Ť�d�ʂ̏㏸��H�{�𑝂₵pH��ቺ������t�ɓd�ʂ̒ቺ��H+�����炵pH���㏸�����顂��̌��ʤ�d�ʂ͇@�ƇA�̎��G�}�T�C�N���Ɍ���I�ȉe����^���顎��G�}�T�C�N�����������邩���U���邩�̋��E�����߂�d�ʂ��������E�d�ʂł��顐������E�d�ʂ��ڂȓd�ʈ�ł�H�{�̋��������Ҍ��ɂ�錸�����x������PH���㏸���ċǕ��A�m�[�h�͍ĕs���ԉ����Ǖ����H�͒�~���� �������E�d�ʂ��E�H������ܕ��H�ȂNjǕ��A�m�[�h�̕ǂ̒��x����Ȃ킿�w�I�����ɂ���ĕω�����͎̂��̂悤�ȗ��R�ɂ�顂��Ȃ킿��E�H�̊w�I�����͂����ܕ��H�ɔ�ׂĊɂ��̂Ť�s�b�g�A�m�[�h���������ێ����邽�߂ɂ͂����ܕ��H�����呬�x�ł̋����C�I���̕⋋�i�A�m�[�h�n���j��K�v�Ƃ��顂��̂��߂����������J�n�����s�b�g�͐�����������t�ɂ�����~�����悤�Ƃ���Ƃ��͏��Ȃ��J�\�[�h���ɂł��ޡ���̂��ߍE�H�̐������E�d�ʂ͓����ޗ��̓������ɂ����邷���ܕ��H�̂�����K�������Ȃ� |
 |
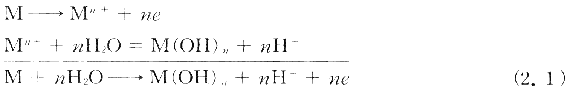 |
 |
�i3�j�E�H�̖h�~
�E�H�̖h�~�ɂ͎��̂悤�ȑƂ���
�@�ύE�H�|�̑I��F�E�H�d�ʂ����߂����N�����̔疌�����^�͍|�\�ʂ���ɐ���ȂƂ��̂ݗL���ł��顈ٕ��Ȃǂ�������������ܕ��H�I�ɍE�H����������Ǝv��ʔ�Q���邱�Ƃ�����̂Œ��ӂ���Mo�����킹�ċ��������^�����萫���傫���
�A���̎_�����̒ጸ�F�E�H�d�ʈȉ���ł���E�H�̐������E�d�ʈȉ��ɂȂ�悤�Ɏ_������ጸ���ł������߂Č��ʓI�ł��顗n���_�f���_���܂ɂȂ��Ă���n�ł͒E�C���邾���ōE�H��h�~�ł��邱�Ƃ�������ϋɓI�ɃJ�\�[�h�h�H��K�p���d�ʂ�����������{�I�ɍE�H��h�~�ł���
|
�����ܕ��H |
 |
�����ܕ��H�̖h�~
���̂悤�ȕ��@�����ʓI�ł���
�@�E�s����pH�̒Ⴂ�ϐH���̍����ޗ���I�肷�顂�������Cr�̔疌�����^�݂̂ɗ���Ƥ���ꂪ�j��ꂽ�Ƃ��̗n�𐫂��傫����v��ʕ��H���邱�Ƃ�����̂Ť���n�̗n�𐫂���������Mo�Ƃ̃o�����X�ɔz������
�A�����܂̏�Ԃ���� �p�����Ԃ��ɘa�����顏d�ˍ��킹�\�����ɗ͔������ނ����Ȃ��Ƃ��͕��H�̔����O�ɂ����܂��J�������
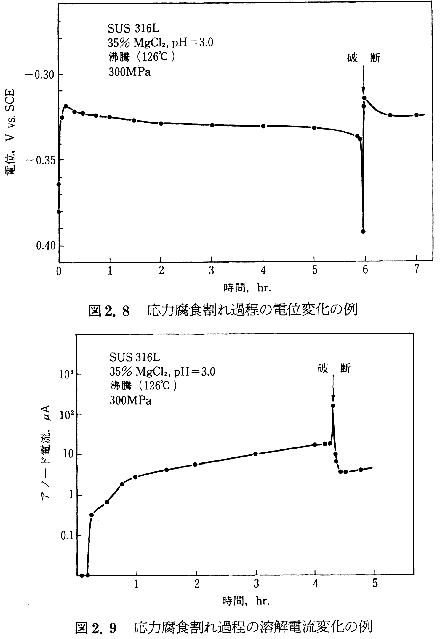
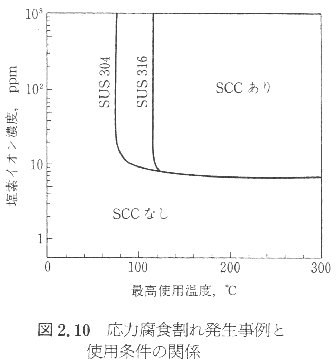
| ���͕��H���� �����n���������e���͓��̐ÓI�Ȉ������͂�����Ԃœ���̕��H�����ɂ��炳���Ƃ��������錻�ۂ����͕��H����iSCC�j�Ƃ����SCC�̓����Ƃ��ẮC�@����̍ޗ��Ɗ��̑g�ݍ��킹�ŋN���顇A���ꕔ�ȊO�͐���ȕ\�ʂ�ۂ¡�B����͓���̂��ׂ�ʂɉ����Đi�W���顇C�ї�����Ɨ��E���ꂪ���顇D�j�ʂɓ��L�̖͗l�������i�Ƃ��Ɋї�����̏ꍇ�̐�`�͗l�j��E���ꂪ�������Ȃ��Ȃ���E���͂����݂��顇F�����ߒ��Ɠ`�d�ߒ��ɕ������顇G�J�\�[�h�h�H�Ŗh�~�ł��顂Ȃǂ��������� ���͕��H����Ƃ��Ăͤ�Â����物���̎��G����i�A�����j�A�ɂ��SCC�j���m���Ă�������ߔN�Ƃ��ɑ傫�Ȗ��ƂȂ��Ă���I�[�X�e�i�C�g�X�e�����X�|�̉��������ł�SCC�𒆐S�ɂ��Ĥ��Ƃ��ĕ��H�̖ʂ��炻�̌��ۂ��l�@���� �Z��MgCl2���ł�SUS316L�Ԃ̊���ߒ��̓d�ʕω���}2.8�ɤ����A�m�[�h���J�\�[�h���番�������������g���ē�������̗n��d���̕ω���} 2.9�Ɏ�������ꂪ�������邽�߂ɔ����̌��E�d�ʂ���d�ʏ㏸���K�v�Ȃ��Ƥ���ꂪ�`�d�ߒ��ɓ���Ɨn��d���̂��߂ɓd�ʂ��ቺ���邱�Ƃ��킩�顂��̂悤�ȔZ��MgCl2����SCC�͍E�H������ܕ��H�ȂǑ��̋Ǖ����H�킸�疌�j�璼�ڊ���`�d�ɓ��邪��ʏ�悭�������Z�x���������ł͍E�H�Ȃǂ̋Ǖ����H����ɋN���褋Ǖ��Z�k�ɂ��Z���������̐����Ɛ،����`���ɂ�鉞�͏W������s����SCC�Ɏ���̂����ʂł��顂��̂��ߎ��n�ł�ppm�I�[�_�[�̂���߂Ĕ����������ł�SCC�����������ƂȂ顔M�� �����p������Cl-�Z�x����x�Ɖ��͕��H���ꔭ�����ᕪ�z�̊W��}2.10�Ɏ���� |
 |
 |
�X�e�����X�|�̉�����SCC�̖h�~
���̂悤�ȕ��@���Ƃ���
�@��SCC�ނ̑I��FMgCl2�^SCC�ɂ͍�Ni�^�C�v����������E�H�^�ɂ͂ނ���ŏ��̐H�E�̔�����h����Mo�^�C�v���L���ł���
�A�J�\�[�h�h�H�̓K�p�F�J�\�[�h�h�H�ɂ��d�ʒቺ�����ʓI�ł���
���H��J
��C���ɂ����ꂽ�����ޗ��ɌJ��Ԃ����͂���������Ƥ�����͂ƌJ��Ԃ����Ɉˑ����ċ@�@�I�Ȕ�J������邱�Ƃ͂悭�m���Ă��顂���Ɠ��l�ɤ���H�������ŌJ��Ԃ����͂����ׂ����Ƥ���̔�J���ꂪ��w�������ꤔ�J���x���������ቺ���顂���ɤ��C���ł̔�J���ۂŌ����銄����E���́i����ȉ��̉��͂ł͂�����J��Ԃ����������Ă�����Ȃ��j���ϑ�����Ȃ��Ȃ褂���߂ĒႢ���̓��x���ł��j��Ɏ��顂��̂悤�ȕ��H�����ŋN���镅�H�Ɣ�J���d�ꂽ�j�ۂH��J�Ə̂���
���H��J�ł͌J��Ԃ����͂ɂ�邷�ׂ�ɂ���Đ������銈���ȐV���ʂ��A�m�[�h�ƂȂ褎��ӂ̃J�\�[�h�Ƃ̊ԂŌ`�������Ǖ��d�r��p�ɂ���ăA�m�[�h�n�������i����顂��̗n���@�\�͂����ܕ��H�ȂǑ��̋Ǖ����H�Ƌ��ʂł��褊�{�I�ɂ͉��͂̉e�����Ȃ��Ă��i�s���顂���Ɉꂽ�ꂪ��������Ɗ����[�֕����͂��W������̂Ť���̗��҂����܂��Ċ�����E���͂��Ɍ��܂Œቺ���邱�ƂɂȂ顔�J����ł͊���j�ʂɓ��L�̎Ȗ͗l�i�X�g���C�G�[�V�����j���ϑ�����邪����H��J�ł͕��H�n���ɂ�肱�ꂪ�s���ĂɂȂ邱�Ƃ����顂܂���������ɂ���Ă͊���T�����ɑؗ����镅�H�������ɂ�餂����ь��ʂɂ���Ď��i�K�̊��ꂪ��w���i�����
���H��J�̖h�~
���̎�i���L���ł���
�@���ꔭ�����Ԃ�x�点�餍����x�ނ�I�肷�餔M�����i�\�ʂɈ��k���͂��c�������鍂���g�ē���Ȃǁj��\�ʏ����i������߂����Ȃǁj�ɂ��ޗ��\�ʂ̋��x�����߂餐،����`���r�����͏W��������顂Ȃǂ����ʓI�ł���
�A���ꔭ����̕��H�ߒ���h�~��}�����餃J�\�[�h�h�H�̓K�p��C���q�r�^�[�̓Y���Ȃǂɂ�褕��H��}������Α�C���̔�J���ۂƓ����x�܂ʼnł��顂������J�\�[�h�h�H�ł͉ߖh�H�ɂ�鐅�f�Ɖ��ɒ��ӂ���
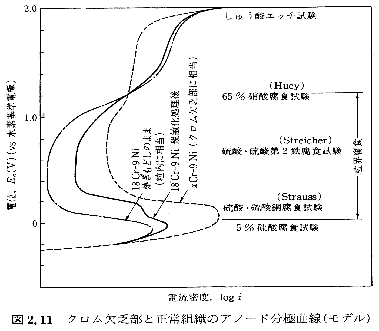
| ���E���H ���p�����͂��ׂđ������\�������Ă��邪����̌����̗������قƂ�Ǖ��H���Ȃ��������ɂ�������炸���E���I��I�ɕ��H�����������o���o���ɂȂ镅�H���������ʓI�Ɍ����̗��E�͋Ìł���т��̌�̔M�����̉ߒ��ɂ�����s�����̕ΐ͂₻��ɔ��������ɂ���ė����ɔ�בϐH������邱�Ƃ������ ���܂��ܗ��҂̑ϐH���̍������m�ɏo�镅�H�����ɂ��炳���Ɨ��E���I��I�ɕ��H����邱�ƂɂȂ顕��H�����������肫�т�����ΑS�ʕ��H�ƂȂ邵��}�C���h�Ȃ�Ί��S�ϐH�������̂Ť������̏ꍇ�����E���H�����݉����邱�Ƃ͂Ȃ�����E���H�͂���߂ċ����g�D�ˑ����̋������H�ł��邽�ߤ�Ƃ�������������q�ɂ̂ݒ��ӂ��s�������ł��邪���������݂�Ε��H���������E�ɂ̂ݕ��H�����������͕��H�����Ȃ����傤�ǂ悢�����ɂ��邽�߂ɐ����镅�H�Ȃ̂Ť����Ӗ��ł͊����q�ˑ����̋������H�ł���Ƃ������顗��E���H�͎�Ƃ��ăX�e�����X�|��A���~�j�E�����ओ������Ȃǂ̍����n�ɐ����邪��I�[�X�e�i�C�g�X�e�����X�|�Ɍ�������̂��ł��d�v�ł���̂Ť����ɂ��čl�@����304�C316�Ȃǂ̃I�[�X�e�i�C�g�X�e�����X�|��650���O��̉��x�ɂ��炳���ƊܗL����C���N�����𒆐S�Ƃ���Y����M23C6�����������E�ɐ͏o���顂��̌��ʤ���E�ߖT�ɃN�������R�w�������������E�̑ϐH�������顂��̂悤�ȔM�����������s�q���Ə̂���n�ڎ��ɗn�������ɗאڂ���M�e�����ɗ����Ɍ���顃N�������R���̃A�m�[�h���ɋȐ��𐳏�g�D�Ƃ̑Δ�̂��Ƃɐ}2.11�ɖ͎��I�Ɏ�����s����s���Ԉ悩��s���Ԉ�ɂ����Ĥ����ȃX�e�����X�|�� �ł������ꂽ�ϐH���������̈�Ť���E�ɑ�������N�������R�S�̕��H�������̐���g�D�ɔ�ׂĒ������傫���Ȃ邱�Ƃ��킩�顗��E���H���͗��_-�� �_����������_-���_���S�����65���Ɏ_�����Ȃǂɂ���ĕ]������邪������͂���������̓d�ʈ�Ŏ�������Ă��� |
 |
���E���H�̖h�~�@
�@��C�X�e�����X�j���g���Y�����������Ȃ��
�ATi�CNb����̈��艻�^���g�p���C�������ɗD��I�Ɍ������������ɋψ�ɕ��U�����ăN�����Y�����̐�����j�~����
�B1,050���t�߂̍�������}�₷��n�̉��M�����ɂ��C�𗱓��Ɍŗn���������E�ւ̐͏o��h���Ȃǡ��Ƃ��čޗ�������̑��{�����
�E�������H
�����n�������̐������������H����i���ꂽ�悤�Ɍ����j��c��̐������@�B�I�ɂ��낢�w�ɕω����镅�H�`�Ԃ�������|�����n�ɑ���������̒E�������H���ł��L���ł��邪����Ɏ��p�ޗ��̒��ł͂˂��ݒ��S�̍��������H���悭�o������顂܂�Ti-Pd�����̕\��Pd�Z�x�̓}�g���b�N�X�ɔ�הZ�k����Ă��褑ϐH�\�͂̌���Ɉ���Ă��邪���������̒E�������H�̉��p�ł���
�i1�j�E�������H
�C�����邢�͒W�����g�p���鉩�����̗�p�ǂɑ�������ꤓ�����Ƃ������E���̂��낢�E�����w���c����������I��I�ɗn�o����Ƃ�����Ƥ��������n�������������瓺�݂̂��Đ͏o����Ƃ���������邪���҂̕����L�͂ł��顂��̏ꍇCu�̐͏o���������H�̃J�\�[�h�����Ƃ��Ȃ�̂Ť���H�͂܂��܂����i����顒E�����w���ψ�Ȍ����Ɏc��w��E�����ƕs�ψ�Ƀv���O��Ɏc�����E���������邪��O�҂͑S�ʕ��H�̌��ʂɤ��҂͍E�H�ȂNjǕ����H�̌��ʂɑΉ�����
�E�������H�̖h�~
���ǂ̂Ƃ��뉩�����̂��̂̕��H��h�~���邱�Ƃɂ��顈����ܗL�ʂ̒ቺ�i15���ȉ��j�Sn�̓Y���Ȃǂ��L���ł��顂����Cu�|Ni�n�i�L���v���j�b�P���j�ւ̍ގ��ύX�Ȃǂ��Ƃ���
�i2�j���������H
�˂��ݒ��S�ł͊ܗL�����C��������}�g���b�N�X���ɍ����̖Ԗڍ\�����Ƃ��ĕ��z���顂��ꂪ��r�I������肵�����x�ŕ��H�����ƕ\�ʂɍ����w���c����ꌩ���S�������ɕω������悤�ȗl����悷�顗�p���𑗂�|���v�Ȃǂɂ悭�����額����w���`�������ƕ��H�̃J�\�[�h�����̏�Ƃ��Ă���߂Č��ʓI�ɍ�p������̌�̕��H�𑣐i���顂��̋@�\�͑O�q�̒E�������H�Ƃ����ʂ�����̂�����C�������̖Ԗڍ\��������Ă��Ȃ����S�b���S�Ȃǂł͍��������H�͔������Ȃ��
�G���[�W�����R���[�W����
�������t�̗̂����ɂ��ُ핅�H��ő̂܂��͉t�̂̏Փˤ�Ռ��ɂ�镅�H��C�A�̕���ɂ��Ռ����H��ő̗��q�ܗL���̂ɂ�門�Օ��H�ȂǤ�@�B�I���C����դ������Ռ��ɂ�蒘�������i���ꂽ���H���ۂ̂��Ă��������
�`�Ԥ�����ꏊ�Ȃǂ̈Ⴂ����t�H�G���[�W������X�����[�G���[�W������������H��z�������H��C�ߕ��H��Ռ����H��L���r�e�[�V�����G���[�W�����ȂǤ���܂��܂Ȗ��̂�����ꂽ���������݂��顂����͂���߂ċ@�B�I�����ɋ߂��i���H�̗v�������Ȃ��j���̂��炫��߂ĕ��H���̂��̂ɋ߂��i�@�B�I�����̓x�������Ȃ��j���̂܂ōL�����z����
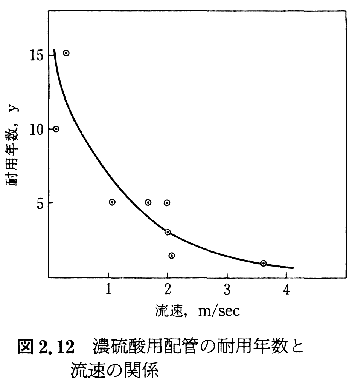
�ϖ��Ր��̂悤�ȋ@�B�I�����͂قƂ�Ǎޗ��Ƒ��葤�̍d���̍��ɂ���Č��܂�ƍl���Ă悢����������ĕ��H�̉e�������Ȃ��@�B�I���Ղ̈��q���x�z�I�Ȍn�łͤ�ł��邾�����葤���d���ޗ���I�肷�邱�Ƃ���{�ƂȂ顂��̌����͕��H�̉e�������܂��������ł����ʂŤ�����ϐH���ƍd�������킹�������ޗ���������ł�����悢��Y�f�|�̔Z���_�ɂ��s���Ԕ疌�͐ÓI�ȏ����ł͑ϐH���������ꤎ��p�ޗ��Ƃ��ď\���Ȕ\�͂����顂��������_��������ԂɂȂ�Ƃ��̗����ɉ����ăG���[�W�������N������������ł͎������ɒ[�ɒZ���Ȃ顐}2.12�ɔz
�Ǔ��̗����Ǝ����̊W����������̂悤�Ȕ�r�I�_�炩���疌�̑����͊_���ł̉��̕s���Ԃɂ��������l�̃G���[�W�����̎��Ⴊ�m���Ă��顈���Ti�̕s���Ԕ疌�͔�r�I�d����ʏ���������ɏՌ����H����悤�ȗ�p��Ɏg�p���Ă��\���Ȑ��\������������������͂����܂ł����ΓI�Ȃ��̂Ť���葤������������čd���Ȃ��͂蓯�l�ɃG���[�W�������顐}2.13�ɐp�X�����[�ɂ��Ti���|���v�ɐ������X�����[�G���[�W�����̗���������ʂɤ�疌�^�̍ޗ��͕��H�ɑ��Ă͂悢���\����������ꂽ�ϐH���������Ăऋ@�B�I���Ղ̉e������G���[�W�����ɂȂ�Ƌ}���ɐN�H�����Ⴊ�����
 |
 |
�G���[�W�����R���[�W�����̖h�~
���n�̑ϖ��Ր���ϐH�����܂߂������I�ȑσG���[�W�����������ƂɓK���ޗ���I�肷�邱�Ƃ��d�v�ł���
| ���f�Ɖ� �Y�f�|������͍|�Ȃǂ�����̊����Ő��f���z�����Ɖ��⊄����邱�Ƃ�����������͕��H�Ȃǂ̕\�ʔ����Ő����������q�f���|���Ɋg�U���Ċi�q���ו��t�߂ւƏW�Ϥ�z��������w�����Ȃǂ̃v���Z�X���o�ĐƉ���c�ꤊ���Ȃǂ�������ƍl�����題Â��̓{�C���[�̤�����Ɖ����L���ł��邪��ߔN������͍|�̔��B�ƂƂ��ɗ������f���͊����x��j��Ȃǂ̑������傫�Ȗ��ƂȂ��Ă���� ���f�Ɖ�����͍|���ւ̐��f�`���[�W�ɂ���đ��i�����̂Ť���̂悤�Ȉ��q�͑��i�v���ƂȂ顇@�J�\�[�h���ɁF�I�[�X�e�i�C�g�X�e�����X�j�̏ꍇ�Ƃ͋t�ɃJ�\�[�h���ɂ�����𑣐i���顇A���f���������̐G�}�ŁF������Бf�ȂǤ���f���q�̍Č�����W����|���ւ̐N���𑣐i���顇B���������F�|�\�ʂł̐��f�K�X�̔�����U���W����|���ւ̐N���𑣐i���� ����h�~��Ƃ��Ăͤ�@���̓��x���������顇A�G�}�ŕ�����������B�C���q�r�^�[�Y���Ȃǂɂ�蕅�H���x�������顇C���̒Ⴂ�ޗ��ɓ]�����顇D�R�[�e�B���O�Ȃǂɂ�������Ւf���顂Ȃǂ��Ƃ��� ���f�Ɖ��͐��f�Ƃ̐e�a�͂̑傫�����̋����ł������顐��f�Ɖ������`�^���Ɍ����鐅�f�����̋����g�D�𐳏�ȑg�D�Ƃ̑Δ�̂��Ƃɐ}214�Ɏ�������̎���͗L�@�_�ipH3�j200���̏����Ŕ������5�N�̎g�p�Ő���ppm�̐��f���z������ł���� |
 |
���������H
�ۤ���Ѥ�y��Ȃǂ̔��������֗^���镅�H���̂��邪��L�`�ɂ͑��ނ⌴�������Ȃǂ̐����̍�p�܂ł��܂߂Ă����ꍇ����������������܂ސ����͂��ׂĎ_���Ҍ���p���c��ł��褋����̕��H�Ɋ֘A����_���Ҍ��n�Əd�Ȃ�ꍇ�������̂Ť�������̐��������H�Ɋւ���͂��Ȃ葽������̍�p�ͤ�@�������̑�Ӊߒ����邢�͑�ӎY�������H�̃A�m�[�h�������邢�̓J�\�[�h�����Ɋ֗^������𑣐i���顇A�����̂���т��̑�ӎY�����X���C���ƂȂ��ĕ��H�̊w�I���q�Ɋ֗^���顂Ȃǂ̋@�\�ɂ����̂Ť�����������ڋ����H����킯�ł͂Ȃ�������̏ꍇ�@�ƇA�͓����ɋN���褔��������H�ƒʏ�̓d�C���w���H�����݂Ɋ֘A�������đS���H���\������
���������H�͗��_���Ҍ��ۤ�����ۤ�S�ۤ�S�_���ۤ����ю��R�C�����̍D�C���ۂȂǂɂ����̂��d�v�ł��顗��_���Ҍ����͎��R�����ɕ�
�ՓI�ɐ������錙�C���ۂŤ���_�����Ҍ����ăG�l���M�[�Ă��褑�ӎY���Ƃ��ė������f�����ċ����H�����顗�p�����C���Ȃǂɂ�����K���ԕ��H�ɑ�Ȃ菬�Ȃ�֗^���Ă���ƍl���Ă悢�
�C�����̃X�e�����X�|�̎��R���H�d�ʂ��������㏸����E�H�₷���ܕ��H�����i����錻�ۂ͌Â�����m���Ă���������ꂪ�D�C���ۂ̑�Ӓ��ԎY���ł���ߎ_�����f�̎_����p�ɂ�邱�Ƃ����炩�ɂ��ꂽ�
�������H
�L�`�ɂ͍����ŋN����_���������N�Y���������f�N�H�����ɂ͗n�Z�����H��_�I�_���H�Ȃǂ̂��č������H�Ə̂���邪������ł͂����銣�H�̔��e�ɓ���O�҂ɂ��čl�@����
�i1�j�_��
�����������Ŏ_�f�ɐڂ���Ɖ��x��_�f������_���������̎��R�G�l���M�[�̑傫���ȂǤ���ꂼ��̔M�͊w�I�����ɉ����Ď_������_�����ɕω�����
���̔����͎��H�Ɠ����悤�ɓd�C���w�I�Ȕ����ɂ���ċN���褎_�����w��ʂ��ẴC�I���d��������ѓd�q�d�����̌��ˍ����ł��낢��ȑ��x�_�I�@�\���o�����顒ʏ�����������_�����疌���ی쐫��L����Ƃ�������ʂ��Ĕ����Ɋ֗^��������C�I������ю_�f�̈ړ����W������̂Ť�_���d�ʑ��ʂ��Ȃ킿���H�ʂ͎��ԂƂƂ��ɒቺ���Ă��顎_���疌�̖��������悭�k���ȑώ_���疌���`������ꍇ����H�ʂ����Ԃ̕������ɔ�Ⴗ�餂�����������������藧���Ƃ�������疌�ɕی쐫���Ȃ��������餎_���������X�Ɣ�����E������悤�ȏꍇ�͕��H�ʂ����Ԃɔ�Ⴕ�����I�ɑ��傷��i�������j�悤�ɂȂ�Cr�CAl�CSi�Ȃǎ_�f�Ƃ̐e�a�J���������f�͗ǍD�ȑώ_���疌�����̂Ť�����̑ώ_�������̎�v�ȍ\�������Ƃ��ė��p�����
�i2�j����
�����������ŗ������܂ޔR���̔R�ăK�X��E���v���Z�X�K�X�ɐڂ���Ɨ���
���H���顗��������͎_�������Ǝ��Ă��邪���ʂɗ������͎_�����ɔ�חZ�_���Ⴂ��C�I���Ȃǂ̊g�U���x���傫����k����������������Ȃǂ���ϐH������蕅�H���₷����Ƃ��Ɏ_�f�����̒Ⴂ�����ŗ����̉e�����₷��������̗������f�K�X����舵���E���v���Z�X�Ŗ��ƂȂ顓S�����ł�Al�CSi�CCr�Ȃǂ̓Y�����ϗ������H���̌���Ɍ��ʓI�ł���
�i3�j�Z�Y
�����̈�_���Y�f��^���ɂ��\�ʂɒY����������������ꂪ�����Ɋg�U���Z�Y���N���顒Y�f�̓N�����ƌ������₷�����E�ɃN�����Y���������ėL���N�����Z�x��ቺ������_���◰�������𑣐i������
�i4�j����
�����̒��f�ɂ�蒂�����N���褒����N�����Ȃǂ����č����̑ϐH��������顂Ƃ��ɒ����A���~�j�E�������₷���Al�ɂ��ύ������H����t�^���Ă��鍇���̑ϐH���Ȃ��₷���
�i5�j���f�N�H
�����̐��f�ɂ��|���̃Z�����^�C�g���������꤃��^�������Ėc��Ȃǂ̑����������顃A�����j�A�����������␅�f�Y���H���ȂǤ���������̐��f�K�X�������v���Z�X�Ŗ��ƂȂ顒Y�f�Ԃɑ���Cr�����Mo�̓Y�������ʓI�Ť�e��Cr�|Mo�|���g�p����顐��f�����Ɖ��x���p�����[�^�ɂ��Ċe��Cr�|Mo�|�̎g�p�\���E���`���[�g�����Ď�����Nelson�}���m���Ă���
���p����
ASTM G82�|93��蔲���D
�֓���g����k���F�����\�ʋZ�p�24�433�i1973�j�D
JIS G 0577�|1981����D
�g�䤋v���F���{�����w�35�C151�i1971�j�D
�ēc��|�R�F�h�H�Z�p�26�C25�i1968�j�D
��F�h�I�Z�p�C22�C419�i1973�j�D
T�DSuzuki�CY�DKitamura�FCorrosion�C28�E1�i1972�j�E
T�DSuzuki�CM�DYamabe�CY�EKitamura�FCorrosion,29�C18�i1973�j�D
��C�k���F�h��Z���17�C154�i1968�j�D
T�DSuzuki�CM�DYamabe�CY�EKitamura�FCorrosion�C29�C70�i1973�j�D
���w�H�w����ҁF���ǎ��X�e�����X�|�M���̉��͕��H����g�p���уf�[�^�W�CP�E32�i1979�j�E
���C��F�h�H�Z�p�@29�C176�i1980�j�D
�����h�H�Z�p�֗��C���{�w�p�U���S�ҁC�����H�ƐV����,P79�i1972�j�D
T�DF�DDegnan�FCorrnsion�C15�C326t�i1959�j�̃f�[�^���쐬�D
�J���F�`�^�j�E���W���R�j�E���C31�C167�i1983�j�D
���{�ޗ��w��H�h�H����ψ���ҁF���H��������Ɖ�͋Z�p�CP�E228�i1987�j�D
��J�C�K�F���{�����w��58�C775�i1994�j�D
�k��,��F�h�H�Z�p,35�`56�i1997�j�D
�����̌f�������ɂȂ�悤�ł�����A����������������f��������߂܂��